Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [2, 13]
L'acrylonitrile est largement absorbé et distribué par toutes les voies d'administration ; il est métabolisé par conjugaison directe avec le glutathion ou par oxydation par l'intermédiaire du cytochrome P450 et excrété dans l'urine sous forme d'un grand nombre de métabolites dont les ions thiocyanate et cyanure et la N-acétyl-S-(2-cyanoéthyl)cystéine (ou acide S-(2-cyanoéthyl)mercapturique).
Chez l'animal
Absorption
Chez le rat, l'absorption de l'acrylonitrile est importante par voie orale (95-98 %) et par inhalation (91,5 %). Par voie orale, elle est monophasique avec un pic sanguin atteint après 1 à 3 heures et une demi-vie dans le sang de 61 minutes. Par inhalation, l'absorption est biphasique : une phase rapide qui dure environ 60 minutes et une phase plus lente, jusqu'à la fin de l'exposition, l’absorption pendant ces 2 phases étant fonction de la concentration [14]. La baisse du taux de glutathion provoque une augmentation du taux d'absorption de l'acrylonitrile par inhalation dans les 2 phases [14].
Distribution
Chez l'animal, l'acrylonitrile et/ou ses métabolites sont détectés dans le cerveau, l’estomac, le foie, les reins, les poumons et le sang dans l’heure suivant le début de l’exposition par inhalation [14].
De la même manière, la distribution suite à une exposition par voie orale est rapide dans tous les tissus. Les concentrations les plus élevées sont retrouvées dans le tractus gastro-intestinal, en particulier dans l’estomac [15, 16].
L’acrylonitrile peut se lier de manière covalente aux acides nucléiques, à l’hémoglobine et à de nombreuses protéines tissulaires.
Métabolisme
Indépendamment de la voie d’exposition, l'acrylonitrile est transformé par 2 voies principales (cf. fig.1) :
- conjugaison directe avec le glutathion avec formation d’acide S-(2-cyanoéthyl)mercapturique (ou N-acétyl -S-(2-cyanoéthyl)cystéine, CMA) ; du fait de la grande réactivité de l'acrylonitrile avec les centres nucléophiles, elle peut se faire avec ou sans glutathion transférase. Cette voie est considérée comme une détoxication.
- oxydation par le système de monooxygénases à cytochrome P450 avec formation d'oxyde de cyanoéthylène (CEO), molécule pouvant réagir directement avec les macromolécules des tissus ou être métabolisée en plusieurs métabolites comme les thiocyanates ou l’acide thiodiglycolique ; cette voie est considérée comme une activation.
La voie prédominante est fonction de la dose systémique. La déplétion en glutathion provoque une bascule du métabolisme de la voie (1) vers la voie (2).
Le métabolite majeur dans de nombreuses espèces animales est le CMA. Les métabolites formés par conjugaison avec le glutathion représentent 85 % des métabolites urinaires.
Schéma métabolique
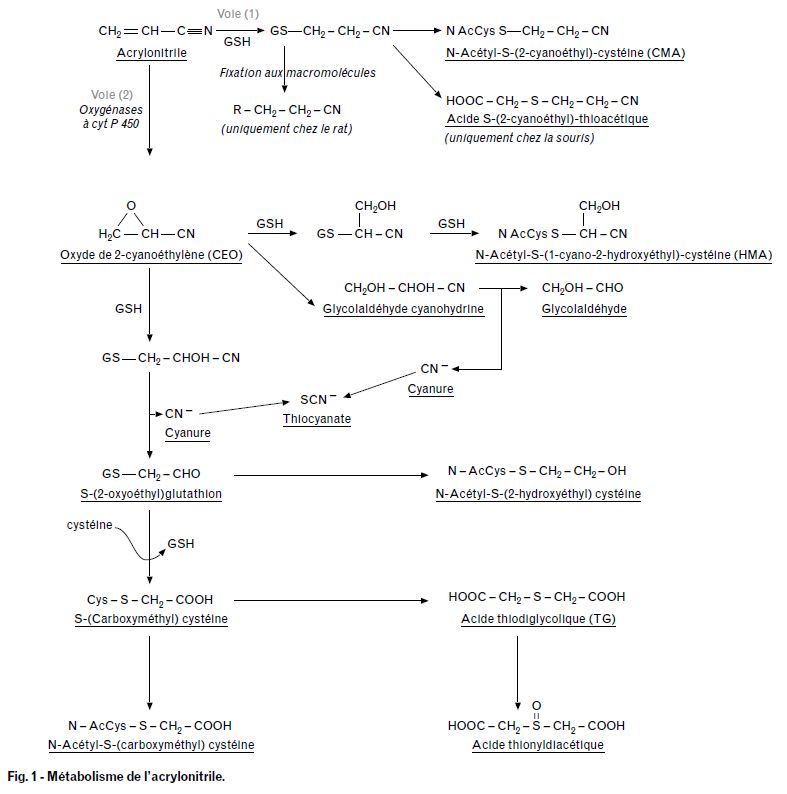
Excrétion
Le rat, après une dose orale d’acrylonitrile radiomarqué, excrète, en 24 heures, 40 % des métabolites dans l’urine, 2 % dans les fèces, 14,3 % dans l’air expiré (4,8 % sous forme inchangée, 9 % sous forme de CO et 0,5 % sous forme d'HCN) ; 27 % des molécules marquées sont présentes dans la bile. L’excrétion totale est de 75 % de la dose initiale après 10 jours.
Cinq métabolites représentent 75-100 % des métabolites urinaires :
- la N-acétyl-S-(2-cyanoéthyl)cystéine (CMA) et l’acide S-(2-cyanoéthyl)-thioacétique issus de la voie métabolique (1) ; ils augmentent de façon non linéaire avec la dose, ce qui suggère une saturation métabolique. Cette voie est prédominante en cas d’exposition à une dose forte à court terme (par gavage ou administration intraveineuse ou intrapéritonéale) ;
- les ions thiocyanates, la N-acétyl-S-(1-cyano-2-hydroxyéthyl)cystéine (ou acide 2- hydroxyéthylmercapturique, HMA) et l’acide thiodiglycolique issus de la voie (2) prédominent lors d’exposition à de faibles doses par voie orale (dans la nourriture ou l’eau de boisson) ou par inhalation.
Après une exposition par inhalation (5 ou 100 ppm soit 11 ou 220 mg/m3, pendant 6 heures, nez seul), le rat excrète durant les 9 premiers jours respectivement 68,5 % ou 82,2 % de la dose dans l’urine, ~ 4 % dans les fèces et ~ 6 % dans l’air expiré sous forme de CO2. Le métabolite urinaire majeur est l’ion thiocyanate (15 -16 % de la concentration inhalée) ; le CMA ne représente que 8 % des métabolites urinaires totaux.
Quand les quantités de glutathion disponibles sont trop faibles ou que la concentration augmente, l’excrétion urinaire de thiocyanate augmente, indiquant une saturation du métabolisme via la conjugaison au glutathion.
Effets de l’espèce
La proportion de conjugués au glutathion en position 2 ou 3 détermine la quantité d'ions cyanures libérée ; les différences dans cette voie seraient responsables des différences interespèces de la toxicité induite par l'acrylonitrile.
In vitro, les microsomes de foie de souris transforment l'acrylonitrile en CEO 4 fois plus vite que ceux du rat qui sont eux-mêmes 1,5 fois plus rapides que les microsomes humains ; ceci se traduit, in vivo, par une formation plus importante de cyanures et une excrétion urinaire de thiocyanates et d'acide thiodiglycolique plus élevée chez la souris que chez le rat et l'Homme.
Production d'adduits : l'acrylonitrile se fixe sur l'hémoglobine in vitro et in vivo en formant des adduits cyanoéthyl, majoritairement par réaction directe avec la cystéine. D'autres adduits peuvent aussi être formés par réaction avec la valine N-terminale (CEVal) ; ils semblent être plus spécifiques de l'acrylonitrile. La quantité d'adduits formés n'est pas linéaire avec la dose d'exposition, elle est le reflet de la quantité d'acrylonitrile circulant dans le sang et augmente avec la consommation de tabac.
Chez l'Homme
L’acrylonitrile est absorbé par voies respiratoire (pour environ 52 % d'une concentration inhalée de 5 ou 10 mg/m3 - 4,2 ppm pendant 4 heures), digestive ou cutanée. Le passage transcutané est d'environ 0,6 mg/cm²/h après application sur peau humaine.
L'acrylonitrile se distribue au niveau de la peau, de l'estomac, des poumons, des reins mais aussi dans les érythrocytes (sous forme de cyanoéthylvaline). Le passage transplacentaire est possible.
Environ 22 % de l'acrylonitrile absorbé par inhalation sont métabolisés par conjugaison au glutathion et aboutissent à la formation d'acide 2-cyanoéthylmercapturique (CMA), principal métabolite de l'acrylonitrile. Pour une moindre part, l'acrylonitrile est métabolisé par oxydation en glycidonitrile (oxyde de 2-cyanoéthylène CEO), hydrolysé en cyanures puis thiocyanates ou conjugué avec formation de dérivés mercapturiques (1-cyano-2-hydroxyéthyl-mercapturique (HMA) et 2-hydroxyéthylmercapturique).
L’élimination urinaire suit une cinétique de premier ordre, sous forme d'acide 2-cyanoéthylmercapturique (CMA) dont la demi-vie d'élimination est de 7-8 heures. Une faible quantité est éliminée sous forme inchangée par voies urinaire et respiratoire [17, 18].
Mode d'actions
Les effets toxiques de l’acrylonitrile sont typiques de l'action d'un nitrile ; l'effet serait dû au clivage de la molécule qui libère des ions cyanures, médiateurs de la toxicité. Cependant le taux de libération et de détoxication des cyanures, la dose d'exposition, la voie d'administration, l'espèce animale et la présence d'autres sites réactifs sur la molécule influencent la nocivité de l'acrylonitrile : les organes cibles sont le système nerveux central (perte de connaissance), les poumons, les reins et le foie (congestion), ainsi que le tractus gastrointestinal (inflammation de la muqueuse et hémorragies).
Toxicité expérimentaleToxicité expérimentale
L'acrylonitrile est toxique pour l'animal en exposition aiguë par inhalation, ingestion ou contact cutané ; il est irritant pour les yeux et la peau et sensibilisant cutané. Une exposition répétée provoque des lésions du tractus gastro-intestinal ou du système nerveux ; après inhalation, il affecte aussi les voies respiratoires. L'acrylonitrile est génotoxique in vitro ; in vivo, les tests sont négatifs ou douteux. Il est cancérogène par voie orale et par inhalation : selon l’espèce, les animaux développent des tumeurs du système nerveux, du tractus gastro‐intestinal, de la glande de Zymbal (*) et/ou des glandes mammaires. Des effets sur les organes reproducteurs mâles et femelles et sur le développement ont été rapportés, y compris en absence de toxicité maternelle.
(*) Glande sébacée présente uniquement chez le rat, au niveau du canal auditif externe
Toxicité aiguë [2, 18, 19]
Les DL50 ou CL50 de l'acrylonitrile sont indiquées dans le tableau I. L'espèce la plus sensible à l'effet létal après exposition par inhalation est le chien, la moins sensible est le singe.
Les signes cliniques apparaissant après une exposition aiguë à l'acrylonitrile et varient peu d'une espèce à l'autre. Ils peuvent être divisés en 4 phases :
- immédiatement après l'exposition, phase d'excitation, larmoiement ;
- suit une phase tranquille avec des symptômes cholinergiques (salivation, larmoiements, pertes urinaires et défécation) ; l'atropine bloque ces effets ;
- ensuite phase convulsive durant laquelle l'animal subit de multiples pertes de connaissance ;
- enfin phase terminale, précédant la mort, avec dépression respiratoire et paralysie.
Voie Animal DL50/CL50 Orale
- Souris
- Cobaye
- Rat
- Lapin
- 28 - 48 mg/kg
- 50 - 85 mg/kg
- 72 - 186 mg/kg
- 93 mg/kg
Inhalation
- Chien
- Souris
- Rat
- Singe
- Cobaye
- 200 mg/m3/4h
- 300 mg/m3/4h
- 470 mg/m3/4h
- 1030-1210 mg/m3/4h
- 990 mg/m3/4h
Cutanée
- Rat
- Lapin
- Cobaye
- 148 - 282 mg/kg
- 226 mg/kg
- 260 - 290 mg/kg
Tableau I. DL50/CL50 de l'acrylonitrile.
Par voie orale, les effets suivants sont rapportés :
- hyperplasie des cellules de Clara chez le rat, suite à l’administration d’une dose de 46,5 mg/kg [15] ;
- diminution de l’hémoglobine, de la concentration en hémoglobine dans les cellules et du nombre de plaquettes chez le rat (gavage, 80 mg/kg) [20].
Irritation, sensibilisation [13]
L'acrylonitrile est irritant pour la peau du lapin (score moyen pour érythème et œdème de 3,6 sur un maximum de 4, effets réversibles) et irritant sévère à modéré pour les yeux (rougeur de la conjonctive, opacité cornéenne diffuse, œdème, non complètement réversibles en 21 jours).
Les études à court terme ont montré une irritation du système respiratoire supérieur (rhinite, hyperplasie de la muqueuse nasale), différente selon les espèces. Ainsi, des cobayes exposés à 575 ppm pendant 4 heures présentent une irritation des voies respiratoires marquée avec toux et exsudat nasal, évoluant en œdème pulmonaire conduisant au décès des animaux (mort retardée). Pour les autres espèces (rat, lapin, chien et singe), seule une légère irritation des voies respiratoires est rapportée.
L'acrylonitrile est sensibilisant pour le cobaye dans le test de maximalisation (95 % de réponses positives pour une concentration de 0,5 % en solution aqueuse).
Toxicité subchronique, chronique [13]
Une exposition répétée à l'acrylonitrile par voie orale ou inhalatoire provoque la létalité dans un certain nombre d'espèces, le chien étant le plus sensible après exposition par inhalation, ainsi que des modifications :
- de poids : perte de poids corporel et augmentation de poids du foie et du cœur ;
- du système nerveux (en lien avec la libération d’ions cyanures) [21] :
- central, cible principale : modifications neurofonctionnelles (faiblesse des membres, convulsions, paralysie) dès 50 mg/kg pc/j chez le rat (5 j/sem pendant 12 semaines),
- périphérique : diminution de la vitesse de conduction dans les nerfs sensitifs (rats, 25 ppm pendant 24 semaines ou 50 mg/kg pc/j pendant 12 semaines) ;
- des voies respiratoires, au niveau de :
- la cavité nasale : hyperplasie, métaplasie et inflammation de l'épithélium respiratoire des cornets nasaux dès 15 ppm (6 h/j, 7 j /sem, pendant 18 semaines, dégénérescence de l’épithélium olfactif à partir de 45 ppm [22],
- des poumons : pneumonie chez les rats mâles à 80 ppm (6 h/j, 5 j/sem, pendant 6 et 12 mois) [23] ;
- du tractus gastro-intestinal : ulcérations de l’œsophage (chien, 16 mg/kg pc/j pendant 6 mois dans l’eau de boisson), lésions prolifératives au niveau de l’estomac non glandulaire (hyperplasie, hyperkératose et/ou métaplasie malpighienne) dès 0,4 et 10 mg/kg pc/j respectivement chez le rat et la souris [24, 25] ;
- hématologiques :
- nécroses et hémorragies dans le foie et la glande de Zymbal du rat, liées à la présence de tumeurs fortement hémorragiques, entraînent une hématopoïèse extramédullaire compensatoire,
- modifications de certains paramètres comme une diminution du niveau en hémoglobine et une augmentation du nombre de réticulocytes chez les rats femelles exposés à 10,9 mg/kg pc/j pendant 23 mois [24], diminution du nombre de lymphocytes chez les rats mâles et femelles (respectivement 20 et 40 mg/kg pc/j pendant 14 semaines) [25].
Des lésions pré-néoplasiques (tumeurs des cellules gliales) sont détectées dans le cerveau de rats exposés par voie orale (4,4 mg/kg pc/ pendant 2 ans, eau de boisson) [26].
Effets ototoxiques [13]
L’exposition de rats à de l’acrylonitrile (2 ou 5 injections sous-cutanées de 50 mg/kg pc) et du bruit (108 dB pendant 8 heures ou 95-97 dB 4 h/j pendant 5 jours) est à l’origine d’une perte persistante de la sensibilité du seuil auditif, en particulier aux fréquences élevées, par comparaison aux témoins et aux rats exposés seulement au bruit [27 à 30].
Une perte de cellules ciliées dans l’organe de Corti est aussi décelée chez ces animaux co-exposés.
Effets génotoxiques [13]
In vitro
L'acrylonitrile est faiblement mutagène pour S. typhimurium et E. coli en présence d'activateurs métaboliques ; l'effet mutagène est plus marqué dans les tests sur levures ou cellules de mammifères en culture (y compris les cellules de lymphome de souris et les lymphoblastes humains) en présence d'activation métabolique et à des concentrations cytotoxiques. Il induit des cassures de l'ADN, des échanges entre chromatides sœurs, des micronoyaux (cellules épithéliales bronchiques humaines, cellules ovariennes et fibroblastes de hamster chinois) et des transformations cellulaires (cellules embryonnaires de hamster, fibroblastes embryonnaires de souris).
Des tests effectués avec le métabolite principal de l'acrylonitrile, le CEO, ont montré que ce dernier est un mutagène direct et serait responsable de l'effet mutagène de l'acrylonitrile en présence d'activateurs métaboliques.
In vivo
In vivo, les résultats de plusieurs tests sont négatifs (létalité dominante et micronoyaux dans la moelle osseuse chez la souris, aberrations chromosomiques dans les lymphocytes humains ou les cellules de la moelle osseuse de souris) ou douteux (synthèse non programmée de l'ADN chez le rat : test négatif dans les hépatocytes ou les spermatocytes, positif dans le poumon et le tractus gastrointestinal).
Les tests pratiqués sur la drosophile ont donné des résultats positifs pour un certain nombre de marqueurs génétiques.
Effets cancérogènes [23, 31]
En 2024, l’acrylonitrile a été classé « cancérogène pour l’Homme » (Groupe 1) par le CIRC sur la base notamment d’indications « suffisantes » de cancer chez l’animal et de preuves mécanistiques. Les études disponibles par inhalation et par voie orale (gavage ou via l’eau de boisson) mettent en évidence la cancérogénicité de l'acrylonitrile chez le rat et la souris, avec des différences d’organes cibles selon l’espèce.
Chez la souris, l’acrylonitrile induit des carcinomes épidermoïdes du préestomac chez les mâles et les femelles lorsqu’il a été administré par gavage [25]. Cette étude rapporte aussi le développement de tumeurs au niveau des ovaires (cystadénomes), de la glande de Harder et des poumons (adénomes/carcinomes).
Chez le rat, l’acrylonitrile est à l’origine :
- par voie orale :
- d’astrocytomes cérébraux et de carcinomes de la glande de Zymbal (eau de boisson, mâles et femelles) [32],
- d’astrocytomes de la moelle épinière (eau de boisson), de carcinomes épidermoïdes du préestomac et d'adénocarcinomes intestinaux (gavage) chez les mâles,
- de carcinomes de la glande mammaire chez les femelles (gavage) ;
- par inhalation :
- d’adénocarcinomes de la glande mammaire,
- d’hépatomes, de tumeurs au niveau de la langue et de carcinomes de la glande de Zymbal uniquement chez les mâles [33],
- d’astrocytomes chez les mâles et les femelles.
Le mécanisme de l'action cancérogène de l'acrylonitrile n'est pas complètement éclairci ; de multiples mécanismes seraient impliqués. Cette substance interfère avec l'ADN par la formation d'adduits (in vitro et in vivo, dans le foie, par l'intermédiaire de son métabolite CEO) et par oxydation (formation de 8-oxodésoxy-guanidine) ; elle augmente également la peroxydation des lipides. Ces deux derniers effets indiquent la présence d'un stress oxydatif (formation de radicaux oxygénés).
Effets sur la reproduction [13]
Fertilité
Une diminution de la concentration et de la motilité spermatique, ainsi qu’une hausse du nombre de spermatozoïdes présentant des malformations, sont rapportées chez le rat (50 mg/kg pc/j, 6 j/sem pendant 12 semaines ou 46 mg/kg pc/j, 6 j/sem pendant 28 jours) [34, 35]. Les animaux exposés présentaient une salivation excessive, une agitation et une irritabilité. De même chez la souris, des signes histologiques et biochimiques de modifications dégénératives sont notés dans les tubes séminifères de souris exposées à 10 mg/kg pc/j d'acrylonitrile pendant 60 jours ; ces modifications s’accompagnent d’une diminution de 45 % du nombre de spermatozoïdes [36]. Aucun signe de toxicité n’est rapporté chez les animaux exposés.
Chez les femelles, le développement des ovocytes et des follicules ovariens est perturbé : augmentation du nombre de follicules atrétiques et inflammation folliculaire, diminution du nombre de follicules pré-implantatoires à partir de 5 mg/kg pc/j pendant 28 jours [37]. Les femelles exposées présentent une diminution de la prise de poids et une diminution de la taille et du poids des ovaires. Lorsque l’exposition dure 2 ans, l’incidence des kystes ovariens et de l’atrophie des ovaires augmente respectivement dès 2,5 et 10 mg/kg pc/j [25] .
Dans une étude sur 3 générations chez le rat (0-100-500 ppm dans l'eau de boisson correspondant à 0~15~40 mg/kg pc/j), l'acrylonitrile n'a pas d'effet sur les capacités de reproduction des générations F0, F1 et F2 à 100 ppm. À 500 ppm, il induit uniquement une légère toxicité chez les parents (baisse du gain de poids et de la prise de nourriture) [38].
Développement
Chez le rat, l’inhalation de 80 ppm du 6e au 15e de gestation entraine une augmentation significative du nombre de malformations fœtales : queue et tronc raccourcis, vertèbres manquantes ou omphalocèle. Le nombre d’implantations, de fœtus vivants et de résorptions, le poids fœtal ou la longueur vertex-coccyx ne sont pas affectés, malgré une diminution du poids maternel aux doses testées (40 et 80 ppm) [39].
Dans une étude 2 générations, l’exposition à 90 ppm d’acrylonitrile engendre une diminution du gain de poids chez les nouveau-nés, du 14e au 21e jour post-natal [22].
Par voie orale, une baisse du nombre de petits est rapportée chez la descendance de souris accouplées après 28 jours d’exposition à 5 mg/kg pc/j, sans toxicité maternelle ; à 10 mg/kg pc/j, le poids de naissance des nouveau-nés est diminué [37]. Chez le rat, l’administration de 65 mg/kg pc/j (gavage, du 6e au 15e de jour de gestation) entraine une diminution du poids fœtal, de la longueur vertex-coccyx, un raccourcissement du tronc et des malformations au niveau des vertèbres, en présence de toxicité maternelle (diminution du poids, hyperexcitabilité et hypersalivation) ; une légère augmentation du nombre de portées avec des malformations de la queue est notée dès 25 mg/kg pc/j [39]. Des malformations au niveau du tronc et de la queue sont rapportées chez les embryons de rats ayant reçu 100 mg/kg pc au 10e jour de gestation [40].
Dans l’étude 3 générations citée précédemment, l'acrylonitrile n'a pas d'effet sur l'embryon à 100 ppm (soit ~8 mg/kg pc/j). A 500 ppm, il est toxique pour les mères (baisse du poids, de la consommation de nourriture et d’eau, diminution de la production de lait) et les petits (baisse de la viabilité et du poids) [38].
Des études in vitro (culture d’embryons de rats avec de l’acrylonitrile) confirment les effets sur le développement avec une diminution dose-dépendante de la croissance des embryons et une augmentation des altérations morphologiques [41, 42].
Effets pertubateurs endocriniens
L'acrylonitrile est classé perturbateur endocrinien de catégorie III dans la base de données DEDuCT.
Pour plus d’informations, se reporter au paragraphe « Effets perturbateurs endocriniens » de la Fiche Toxicologique 0 (https://www.inrs.fr/publications/bdd/fichetox.html) .
Toxicité sur l’HommeL’acrylonitrile est très irritant pour la peau, les yeux et les voies respiratoires. Une exposition aiguë à de fortes concentrations peut entrainer une intoxication systémique avec troubles digestifs et neurologiques pouvant évoluer vers le coma et l’arrêt cardiorespiratoire. L'exposition répétée peut provoquer une irritation cutanée, oculaire et respiratoire ainsi que des symptômes neurologiques centraux. Des eczémas ont été rapportés. Les études de génotoxicité sont globalement négatives. Un excès de risque de cancer pulmonaire est rapporté chez des salariés exposés à l’acrylonitrile, les données concernant l’association avec le cancer de la vessie sont moins concluantes. Les études publiées ne permettent pas de conclure sur la toxicité pour la reproduction de l'acrylonitrile lors d'expositions professionnelles.
Toxicité aiguë [2, 5, 13, 18, 43-45]
Le contact avec de l'acrylonitrile sous forme de liquide ou de vapeurs entraîne des signes d'irritation cutanée à type d'érythème, d’œdème, de prurit, avec apparition retardée possible de brûlures voire de phlyctènes. Des symptômes d’irritation oculaire (larmoiement, conjonctivite) sont également retrouvés. L’inhalation de vapeurs entraîne une irritation des voies respiratoires (toux, dyspnée).
Une exposition à de fortes concentrations d’acrylonitrile par voies respiratoire ou cutanée provoque une intoxication systémique retardée avec une atteinte du système nerveux central (céphalées, vertiges, somnolence, irritabilité, asthénie). Il s'y associe fréquemment des troubles digestifs (nausées, vomissements, voire des atteintes hépatiques). En cas d'intoxication grave surviennent des convulsions généralisées et un coma pouvant évoluer vers l’arrêt cardiorespiratoire.
Toxicité chronique [2, 13, 44-46]
Lors d’expositions chroniques par voie cutanée et/ou inhalatoire, les effets rapportés sont le plus souvent des signes d’irritation cutanée, parfois sévères, ainsi que des atteintes oculaires et/ou respiratoires (toux, dyspnée). Des symptômes généraux variés ont également été décrits, notamment des céphalées, une asthénie, des nausées, des vomissements et des diarrhées, pour des concentrations proches de 5 ppm. Des effets neurologiques centraux à type de troubles du sommeil, d'irritabilité, de troubles de la concentration, proches des troubles mentaux organiques dus aux solvants ou aux métaux, sont également décrits : leur interprétation est délicate en raison des expositions associées ou du manque d'information sur les expositions.
Plusieurs cas d'eczéma de contact liés à l'acrylonitrile ont été publiés [47]. Un auteur rapporte cinq cas de dermite allergique de contact chez des travailleurs de la production d'acrylonitrile, avec des patch-tests cutanés avec l'acrylonitrile monomère dilué à 0,1 % dans la vaseline qui étaient positifs (et négatifs chez les témoins) ; un des sujets se plaignait de paresthésies des doigts et des avant- bras, réversibles à l'arrêt de l'exposition [46].
Une étude de mortalité a révélé un risque accru de décès par pneumopathie chez les travailleurs exposés à des niveaux supérieurs à 3,12 ppm-années d’exposition cumulative et une durée d’exposition supérieure à 14,5 ans.
Une étude portant sur des travailleurs exposés pendant plus de 5 ans à des concentrations d’environ 4,2 ppm n’a montré aucune anomalie hépatique, rénale ou hématologique.
Effets génotoxiques [13]
Les études de génotoxicité sont globalement négatives.
Une étude a mis en évidence une augmentation de la fréquence des échanges de chromatides sœurs dans les lymphocytes de 26 salariés (13 agents de maintenance et 13 producteurs de fibre) exposés professionnellement à l’acrylonitrile et au diméthylformamide, comparativement aux témoins.
Une étude montre une augmentation des cassures simple brin de l'ADN des cellules spermatiques chez 30 salariés exposés à l'acrylonitrile et une augmentation de la fréquence des chromosomes sexuels aneuploïdes chez 9 d'entre eux comparés à des témoins. Les auteurs concluent que l'acrylonitrile entraîne une baisse de la qualité du sperme en induisant in vivo des cassures d'ADN et des non-disjonctions des chromosomes sexuels dans les spermatogonies de salariés exposés [48].
Effets cancérogènes [31]
L'acrylonitrile est classé cancérogène catégorie 1 par le CIRC, les preuves ayant été jugées suffisantes pour l’association avec le cancer du poumon et limitées pour l’association avec le cancer de la vessie.
Dans une étude cas-témoins (2822 cas et 3098 témoins) réalisée dans différentes industries de 7 pays européens (Scélo et al. dans [31]), une augmentation significative du risque de cancer du poumon a été observée chez les travailleurs exposés à l’acrylonitrile (OR = 2,20 ; IC 95 % : 1,11–4,36), après ajustement pour le tabagisme et d’autres facteurs de confusion.
Dans une cohorte rétrospective de 25 460 travailleurs exposés à l’acrylonitrile dans huit installations industrielles américaines (Koutros et al. dans [31]), une augmentation significative de la mortalité par cancer du poumon a été mise en évidence chez les travailleurs les plus exposés (≥ 32 ppm-années ; HR = 1,47 ; IC 95 % : 1,07–2,02).
Dans la même cohorte, il n’a pas été observé d’excès global de mortalité par cancer de la vessie (SMR = 0,86 ; IC 95 % : 0,61–1,17). Cependant, les analyses ont montré un risque accru pour les salariés ayant une exposition moyenne (> 2,56 ppm, 10 ans de décalage ; HR = 2,96 ; IC 95 % : 1,38–6,34), avec une tendance dose–réponse significative (p = 0,02).Effets sur la reproduction
Une baisse significative de la concentration et du nombre total de spermatozoïdes ont été observées chez des travailleurs exposés à l’acrylonitrile [48], sans effet notable sur le volume du sperme, la viabilité, la mobilité ni la morphologie des spermatozoïdes. L’exposition moyenne était de 0,36 ppm pendant 2,8 ans, sans données supplémentaires sur d’éventuelles expositions à d’autres substances [13].
Une étude cas-témoins, réalisée sur 477 femmes exposées professionnellement à l’acrylonitrile, retrouve une plus forte incidence de naissances prématurées et de malformations chez les exposées comparativement aux 527 témoins. En raison des co-expositions à d'autres produits chimiques, il est impossible de conclure sur une éventuelle relation avec l'exposition (ce d'autant que l'étude est peu documentée).
À l’inverse, une étude hongroise menée chez des travailleurs exposés à l’acrylonitrile n’a pas montré d’augmentation globale des malformations congénitales chez les enfants des ouvriers et ouvrières. Cette étude présente toutefois d’importantes limites [49].Cohérence des réponses biologiques chez l'Homme et l'animal
